▶新着記事を公式LINEでお知らせしています。友だち申請はこちらから!
▶ICCの動画コンテンツも充実! YouTubeチャンネルの登録はこちらから!
ICC FUKUOKA 2022 REALTECH CATAPULTに登壇いただき見事3位に入賞した、セルファイバ 柳沢 佑さんのプレゼンテーション動画【ついに大量培養実現! 日本発「細胞の薬」で世界標準をつくる「セルファイバ」】の文字起こし版をお届けします。ぜひご覧ください!
ICCサミットは「ともに学び、ともに産業を創る。」ための場です。毎回300名以上が登壇し、総勢900名以上が参加する。そして参加者同士が朝から晩まで真剣に議論し、学び合うエクストリーム・カンファレンスです。 次回ICCサミット KYOTO 2022は、2022年9月5日〜9月8日 京都市での開催を予定しております。参加登録は公式ページをご覧ください。
本セッションは、ICCサミット FUKUOKA 2022ゴールド・スポンサーの KOBASHI HOLDINGS にサポートいただきました。
▼
【登壇者情報】
2022年2月14〜17日開催
ICC FUKUOKA 2022
Session 7A
REALTECH CATAPULT
リアルテック・ベンチャーが世界を変える
Sponsored by KOBASHI HOLDINGS
柳沢 佑
株式会社セルファイバ
代表取締役社長
2007年東京薬科大学 生命科学部 環境生命科学科卒業。2011年3月まで株式会社リバネスにて企画開発業務に従事。2017年12月 東京大学大学院 化学生命工学専攻にて博士(工学)を取得。2018年3月、平成29年度東京大学工学系研究科研究科長賞・東京大学総長賞。専門は高分子化学、材料化学、ソフトマテリアル、ハイドロゲル。2018年5月よりセルファイバ取締役に就任。2018年6月よりAMED「細胞ファイバーを利用した抗体製造のための高密度連続生産技術の開発」研究開発代表者。2018年10月にNEDO Entrepreneurs Profgram(NEP)に採択され心筋ファイバの創薬応用を志向した収縮力測定システムを開発。2019年6月より代表取締役に就任。
▲
「細胞の薬」で、治せなかった病が治る時代へ
柳沢 佑さん セルファイバの柳沢です。
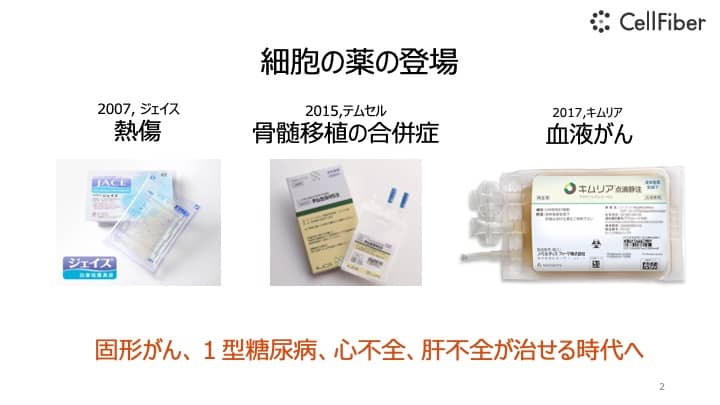
今は細胞が「薬」として使われる時代になっています。
例えば、重症の火傷を負ったとき、骨髄移植で合併症が起きたとき、血液がん、こういうものが細胞で治療可能になってきています。
この後に固形がんや糖尿病、肝不全、心不全、こういったものが実用化されていくことが期待されています。
図の出典:https://www.pmda.go.jp/files/000210025.pdf
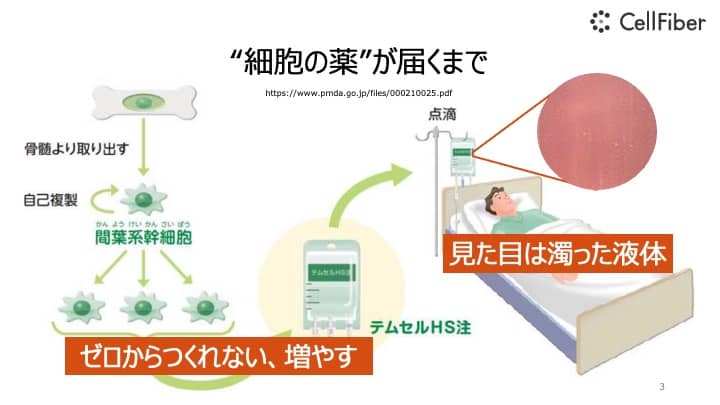
「細胞の薬」といったときに、ちょっとイメージが湧かないと思うのですが、例えば人間は細胞を自分でゼロから作り出すことはできませんので、お薬になる機能を持った細胞を見つけてきて、それを増殖させ、この場合では点滴のような形で患者様に投与するという使われ方がされます。
年間製造量はごくわずかで高額という現実
点滴のバッグの中身を見てみると、その中には濁った液体があります。
その濁った液体の、濁っているものというのは、細胞の粒々が入っています。
ではこれに、どれぐらい細胞が入っているかを見ると、1回に投与される量は1gにも満たないような、ものすごく少ない量です。
たくさん作れそうなものですが、実態として100製品グローバルで上市されているものを計算してみると、年間数100gと推定できます。
その結果として、患者さんは1万人いるのに数百人にしか届いていないとか、それが原因で非常に高額といった現実があります。
なぜ細胞の大量生産ができないのか
では、なぜたくさん作れないのか気になりますよね。
大きく分けて、細胞を作る方法は2つあります。
上はお皿の中で細胞を増やすという、大学や研究室でよく用いられる技術です。
この技術の問題点は、お皿をとにかくたくさん増やしていかなければいけないので、100倍、1,000倍作ろうとすると、とにかく面積を稼がなければいけません。
そうすると、どこかで限界が来ます。
そのため空間的に使おうという「三次元培養」という方法があり、大規模化できます。
一方でタンクが大きくなっていくほど、かき混ぜる力で細胞にダメージがかかってきたりするのです。
これが問題で、産業上実用的な技術になっていないのが現実です。
つまり細胞のいいところは、今までにない治療を可能にするような複雑な機能を担えるところです。
一方で豆腐のように壊れやすく、生肉のように質が変わりやすいという厄介なところがあるのが現実です。
壊れやすい細胞をゲルのヒモに詰めて守る
我々が取り組んでいるのは、ここにお見せしている細胞をゲルのヒモ(細長い繊維)に詰めるという技術で、この解決に用いています。
このスライドが一番重要なのですが、「細胞ファイバ」は何かというと、こういうイメージです。
このブドウを運ぶネットと思ってください。
この中に入っているブドウと比べると1万分の1ぐらい細胞は小さいですが、つまり中身の大事なものを物理的なバリアで守って、一方で酸素や栄養素など必要なものは供給する、こういう機能を担うと、内部にある粒子を守ることができて扱いやすくなるという付加価値があります。
大規模な製造技術の開発に成功
2019年に、この話を同じ場所でさせていただいて、こちらをお見せしました。
▶細胞ファイバ技術で、“誰もが手の届く細胞治療”を実現する「セルファイバ」(ICC FUKUOKA 2020)【文字起こし版】
細胞ファイバを実際に作っているところの動画です。
この時はまだスケールアップがポテンシャルとしてできるというお話でしたが、この3年程度で大規模製造が実際に可能になってきています。
これは、1Lの培地の中で、年間で製造するような量の細胞を実際に培養しているところの動画です。
これをもう少しクローズアップしてみますと、白いヒモが見えるのですが、このヒモの中身に細胞がぎっしり詰まった状態になっています。
一度にたくさん作れることに加えて、例えば通常では10倍ぐらいの培地量で作らなくてはいけないものを、ものすごくコンパクトに作れたり、半自動化されるような仕組みになっています。
水槽の水換えではないのですが、どんどん細胞と培地を入れ換えていかなければいけません。
こういう作業が自動化されています。
「初めて現実的な大量製造方法が見えた」との評価も
世の中に細胞を増やす技術はいろいろあるのですが、規模の点や細胞の質を維持する、コストを抑える、こういうところを満たしていく技術に成熟してきているフェーズに今入っています。
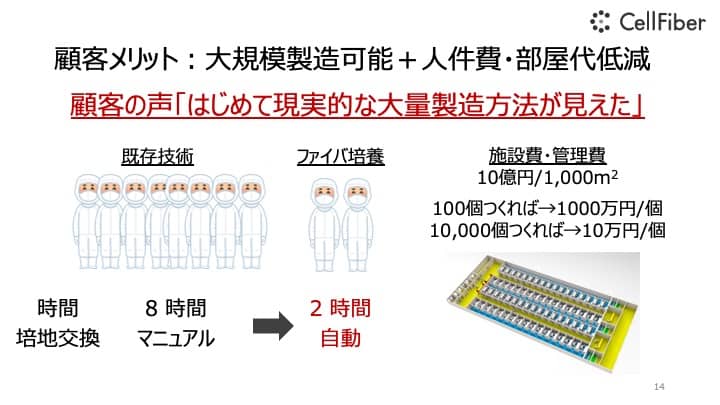
これを代表する声として、「はじめて現実的な大量製造方法になりそうだね」というようなことを言っていただけるところまで今きています。
これをもう少し分解してみると、例えば一気に一度に作ろうとすると、8人がかりで丸1日かけて細胞をお世話・回収しなければいけないところを数人で短時間で完結させられるようになります。また設備を小さくできるのも重要な側面です。
それで、今までこのような研究開発の装置があったのですが、よりお客様のところにも届きやすい安価なお試しキットのようなものや、商用生産に使うような装置を今作り始めています。
本当に世の中に出すまでを5段階としたら、今はこの②から③に移行するような技術を試すフェーズにあって、今まではフィージビリティスタディ(※実行可能性調査)のようなところをやっていました。
これを製造の規模で実際に、原料から最終製品にするところまでを検証していくというチャレンジを2022年にやることになっています。
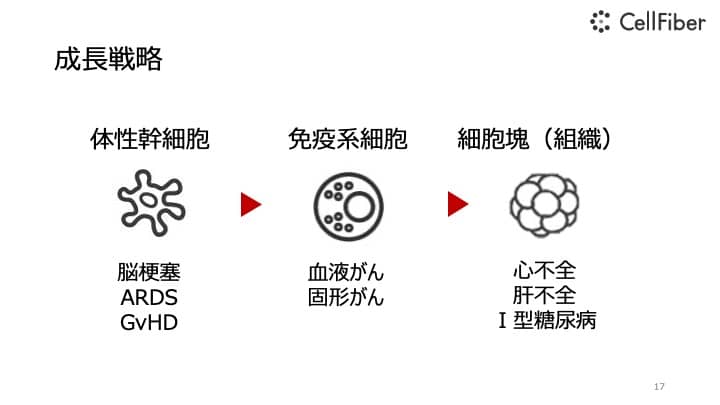
これには3種類ぐらいのカテゴリーがあり、比較的安全な細胞からスタートし、がんの領域になるもの、あるいは組織を置換していくようなものに順次移行していく予定です。
2030年までに100製品のライセンス契約を目指す
ビジネスモデルはライセンスと消耗品販売ですが、一つの製品として実質使われると数十億円規模になっていき、これを2030年までに100製品に到達させるというのが我々の目標になっています。
まだまだこの挑戦は始まったばかりですが、ありがたいことに我々の技術を使っていただける企業、大学も含めて、少しずつ出てきているような状況です。
日本で薬を作り、細胞製造の世界標準を作る
今日はブドウの例えをしましたが、実際にはいろいろと複雑な技術です。これを実行するチームがこの3年間で揃ってまいりました。
日本では、今お薬のだいたい95%ぐらいが輸入されています。
新しいカテゴリーになると、製造技術は全く異なります。
この細胞ファイバというのは、そういう世界の中でまた新しい標準的なものになっていけると我々は信じてやっております。
今日は細胞の薬のお話がメインだったのですが、細胞という非常に機能の高いものをうまく扱うとできることというのは、「培養肉」であったり「ミニチュア臓器」といった発展が見られます。
こういう世界をぜひ実現できたらいいなと思う方に、このセルファイバ を応援していただけたらうれしく思います。
今日は貴重な機会をいただき、ありがとうございました。
(終)
▶新着記事を公式LINEでお知らせしています。友だち申請はこちらから!
▶ICCの動画コンテンツも充実! YouTubeチャンネルの登録はこちらから!
編集チーム:小林 雅/星野 由香里/浅郷 浩子/戸田 秀成/小林 弘美
更新情報はFacebookページのフォローをお願い致します。
≈